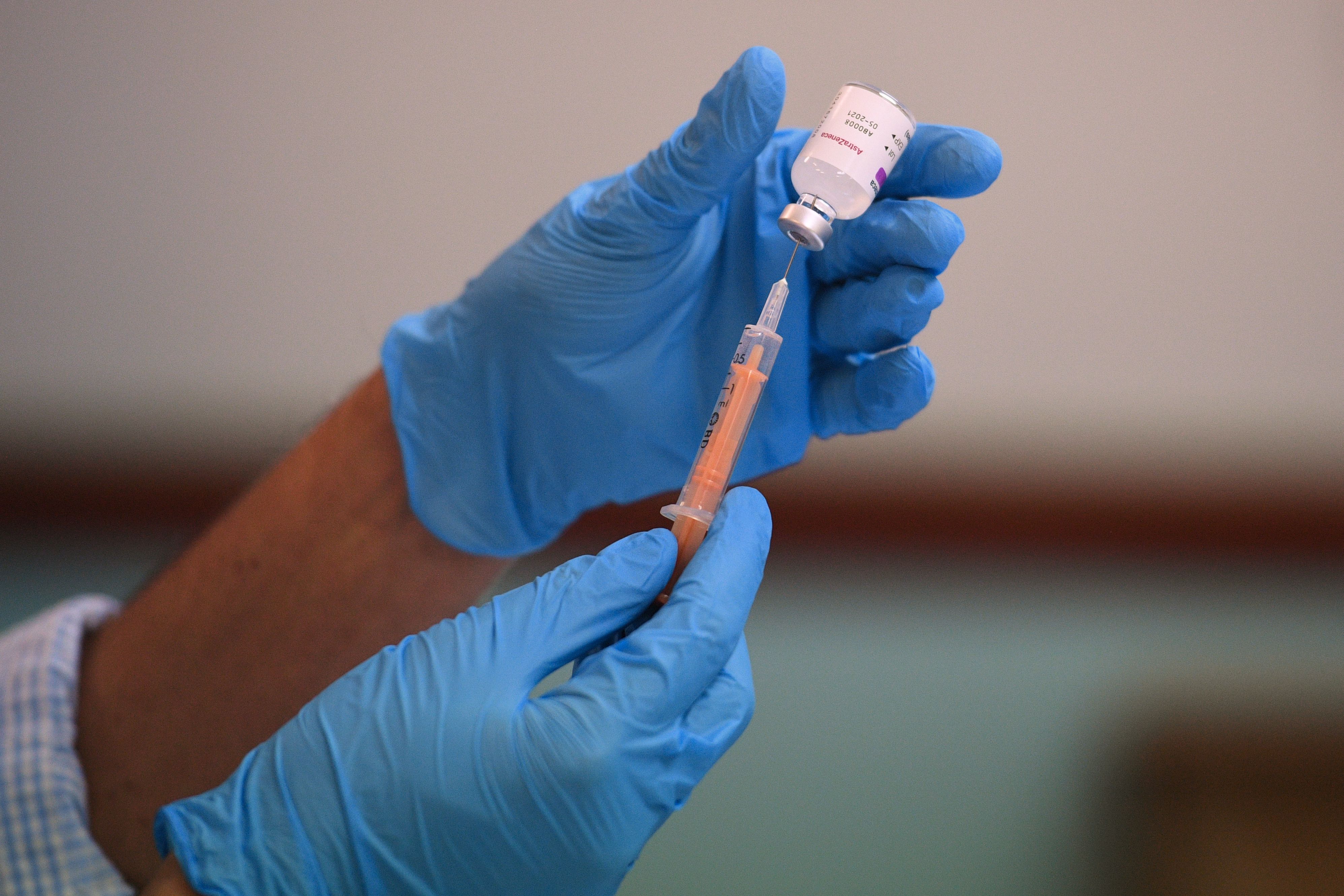
Según el Ministerio de Salud Pública y Asistencia Social (MSPAS), de momento se mantienen acercamientos con los fabricantes de las vacunas AstraZeneca, Johnson & Johnson, Sputnik, Soberana II, Moderna y Pfizer.
Lucrecia Ramírez, viceministra técnica de salud, dijo que entre las dificultades que han enfrentado para concretar las negociaciones se encuentran varios factores, entre ellos que algunos laboratorios solicitaban depósitos por adelantado o la falta de capacidad de producción de las casas farmacéuticas.
Además, otro obstáculo es el hecho que algunas vacunas aún no cuentan con la autorización de entes regulatorios como la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés), la Organización Mundial de la Salud o la Agencia Europea de Medicamentos, comentó la viceministra técnica.
De las vacunas que el gobierno busca adquirir, se encuentran en fase tres Pfizer, AstraZeneca, Johnson & Johnson, Sputnik y Moderna. Esta es la etapa previo a la aprobación de la vacuna y se evalúa la seguridad y eficacia del fármaco. Para ello se aplica a cientos de miles de voluntarios que pueden ser de uno o varios países.
La otra vacuna en la que el gobierno ha mostrado interés es Soberana II, que produce el Instituto Finlay de Vacunas. Esta se encuentra en fase II, en la que se aplica a un grupo de humanos de entre 200 y 500 personas para monitorear seguridad, capacidad imunógena, dosis propuestas y método de administración.
Primer lote
Recientemente el gobierno anunció que a finales de febrero vendría el primer lote de vacunas AstraZeneca que se adquirió mediante el mecanismo Covax. La ministra de salud, Amelia Flores, anunció que en un inicio se prevé vacunar a más 125 mil trabajadores de salud y cada uno deberá recibir dos dosis.
El objeto de estas jornadas de vacunación será proteger de forma individual a quienes están en primera línea de defensa contra la covid-19. De momento, no se observará un efecto en cuanto a disminuir la transmisibilidad o mortalidad de la covid-19, coinciden expertos consultados.
Iriz Cazali, infectóloga de la Asociación Guatemalteca de Enfermedades Infecciosas (Agei), dijo que será hasta que se alcance una cobertura del 60 por ciento de la población cuando se comience a observar una disminución en cuanto a la cantidad de pacientes que desarrollan un cuadro clínico severo luego de contagiarse.
Citó como ejemplo Israel, donde ya se alcanzaron estos porcentajes de cobertura y se ha visto una disminución en los pacientes que requieren hospitalización y en los índices de mortalidad.
Países asumen riesgos
Mario Melgar, presidente del Consejo Nacional de Prácticas en Inmunizaciones (Conapi), explica que los países que suelen tener acceso más rápido a las vacunas son aquellos que, o han financiado la investigación, o las han comprado antes que se publicaran los estudios sobre su eficacia o seguridad.
“Hay países que apostaron por varias vacunas sin saber cuál iba funcionar y las pagaron antes. Guatemala pudo haber hecho eso, aunque desconozco si era posible”, explicó Melgar.
Julio Valdés, exviceministro técnico de salud y exsecretario ejecutivo del Consejo de Ministros de Centroamérica (Comisca), comenta que Guatemala pudo haberse adelantado a comprar vacunas aunque no concluyeran los estudios, aunque el riesgo era preferir una opción y que no tuviera la efectividad deseada.
Valdés señala que los gobiernos son autónomos y la compra de fármacos no está supeditada a que el FDA o la Agencia Europea de Medicamentos den su aval. Sin embargo, las autoridades prefieren esperar estas autorizaciones dado que estas agencias tienen mejores capacidades para evaluar las tecnologías sanitarias.
“Todos los gobiernos son autónomos y no están supeditados a las aprobaciones de la FDA ni de la Agencia Europea de Medicamentos, pero estas entidades regulatorias sí se utilizan como referentes”, explicó.
De momento, la Organización Panamericana de la Salud/Organización Mundial de la Salud (OPS/OMS) reporta 63 vacunas que están en desarrollo clínico. De estas, 34 se encuentran en etapa tres y se encuentran a un paso de su aprobación. La mayoría requiere una segunda dosis entre el día 14 y 28 después de la primera inyección.